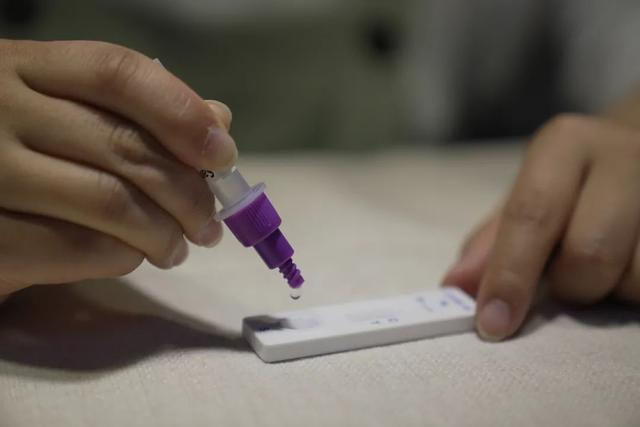
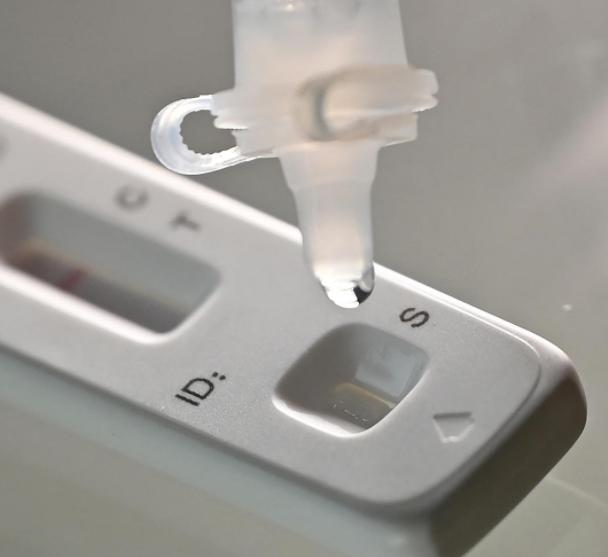
Pada 12 Macth 2022, yangNMPA (SFDA) mengeluarkan notis meluluskan perubahan permohonan untuk ujian kendiri produk antigen COVID-19 oleh Nanjing Vazyme BiotechCo., Ltd, Beijing Jinwofu Bioengineering TechnologyCo., Ltd, Shenzhen Huada Yinyuan Pharmaceutical Technology Co., Ltd, Guangzhou Wondfo Biotech Co., Ltd danBeijing Savant Biotechnology Co.,ltd(Huaketai).Lima produk ujian kendiri antigen COVID-19 telah dilancarkan.
Pada 11 Mac 2022, NHC telah mengumumkan bahawa, untuk mengoptimumkan lagi strategi ujian Novel Coronavirus dan memenuhi keperluan pencegahan dan kawalan COVID-19, Pasukan Komprehensif mekanisme pencegahan dan kawalan Bersama Majlis Negeri memutuskan untuk menambah ujian antigen kepada ujian asid nukleik dan menjadikan "Protokol Aplikasi untuk Pengesanan Antigen (Percubaan) Novel Coronavirus"
Protokol menentukan populasi yang berkenaan untuk ujian antigen:
Pertama, mereka yang melawat institusi perubatan utama dan mempunyai simptom seperti saluran pernafasan dan demam dalam tempoh 5 hari dari permulaan simptom;
Kedua, kakitangan pemerhatian kuarantin, termasuk pemerhatian kuarantin di rumah, hubungan rapat dan hubungan sub-dekat, pemerhatian kuarantin masuk, kawasan pembendungan dan kakitangan kawasan kawalan;
Ketiga ialah penduduk komuniti yang memerlukan pengesanan diri antigen.
Petua: Pengesanan antigen adalah tambahan penting bagi pengesanan asid nukleik, tetapi hasil pengesanan diri antigen tidak boleh digunakan sebagai asas untuk diagnosis jangkitan
Masa siaran: Mac-22-2022